近期,分析化学教研室陈金阳副教授团队在纳米生物传感领域取得多项研究进展,相关成果相继发表在Analytica Chimica Acta, Talanta和Analytical Chemistry等分析化学领域重要期刊上。
5月,Analytica Chimica Acta(《分析化学学报》)在线发表该团队研究成果,论文题为“Self-priming isothermal polymerization engineered in-situ copper nanoparticles generation for one-tube biomarkers sensing”(《自引发等温聚合调控铜纳米粒原位生成的一管式生物标志物检测》)。我院2021级硕士研究生曾莎莎和2022级硕士研究生陈金涛为论文共同第一作者,陈金阳副教授为论文唯一通讯作者,湖北师范大学为论文唯一通讯单位。Analytica Chimica Acta是Elsevier出版社旗下分析化学领域知名期刊、中科院SCI化学大类二区TOP期刊,最新影响因子为6.0。

该研究提出了一种基于自引发等温聚合(SPIP)调控铜纳米粒原位生成的一管式、免标记生物标志物检测新方法。首先,设计了一种由富含腺嘌呤/胸腺嘧啶(AT)的茎环结构和磷代磷酸化修饰的DNA发夹组成的哑铃型底物DNA。当聚合酶启动反应时,底物DNA上交替发生酶促延伸和自折叠过程,产生大量内含重复富AT模板的长双链DNA,最终可实现荧光铜纳米粒的快速生成。利用碱性磷酸酶(ALP)催化去磷酸化反应产生的3'-OH末端作为聚合起始位点,该SPIP调控铜纳米粒原位生成策略成功应用于真实血清样本中ALP的精准检测。进一步研究显示,结合脱嘌呤/嘧啶核酸内切酶1(APE1)触发探针DNA构象转化产生底物DNA,该SPIP方法还可实现APE1的高灵敏度检测。得益于APE1检测的稳健性和简便性,根据细胞APE1的检测结果,该方法能准确区分正常细胞与肿瘤细胞。
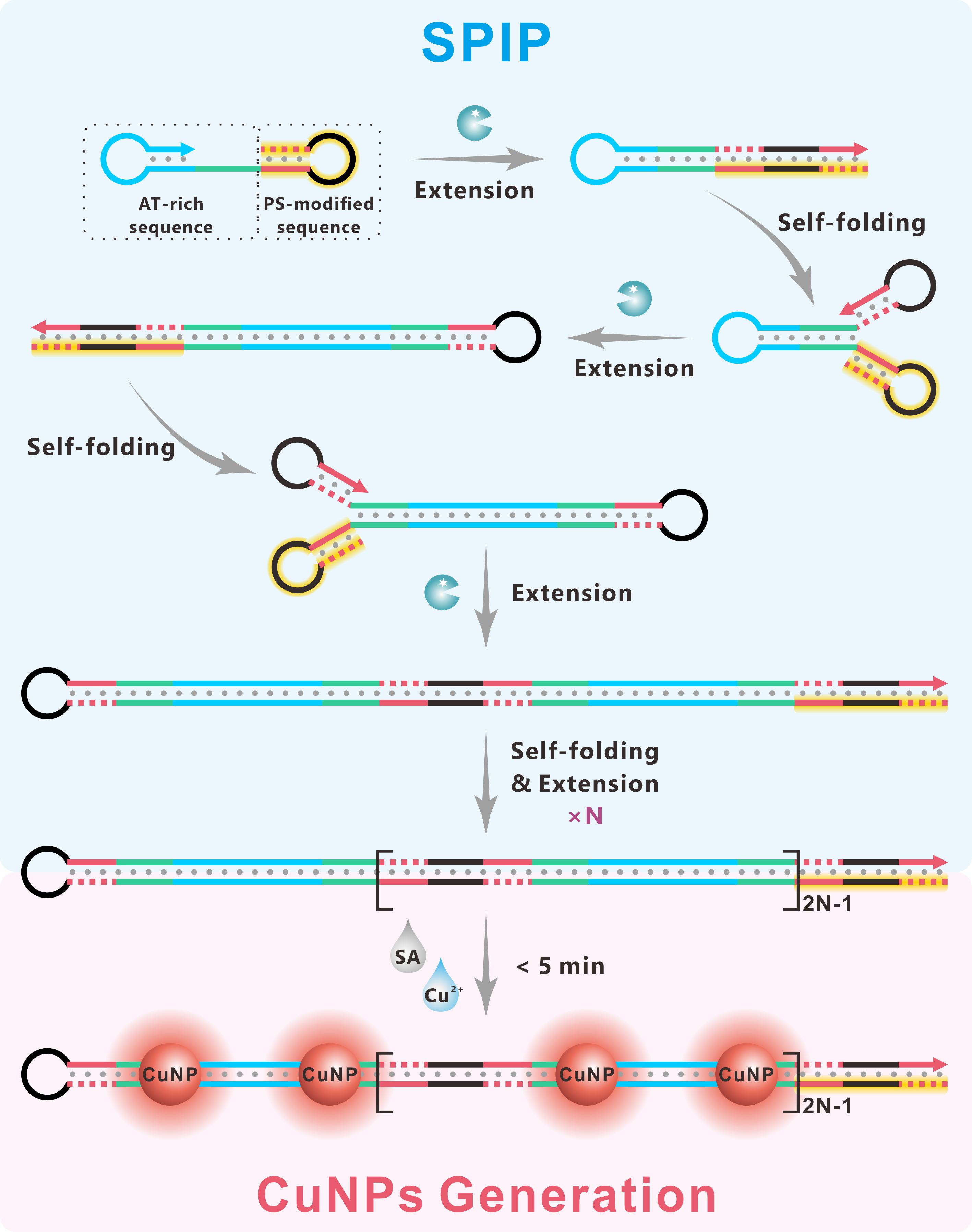
自引发等温聚合调控铜纳米粒原位生成原理示意图
7月,Talanta(《塔兰塔》)在线发表该团队研究成果,论文题为“Palindrome design-guided “single-flap-double-duties” and “dual-enzymes-quadruple-cycles” enabled nano-signal amplification for customized FEN1 sensing”(《回文设计指导“单瓣双功能”与“双酶四循环”赋能纳米信号放大用于定制化FEN1传感》)。我院2022级硕士研究生陈金涛和2023级硕士研究生尚钰慧为论文共同第一作者,陈金阳副教授为论文唯一通讯作者,湖北师范大学为论文唯一通讯单位。Talanta是Elsevier出版社旗下分析化学领域知名期刊、中科院SCI化学大类二区TOP期刊,最新影响因子为6.1。

该研究开发了一种基于定制化靶标识别、指数信号放大和纳米信号转导的FEN1一管式超灵敏检测方法。通过合理的回文序列设计,该传感系统仅需两种DNA底物和一对酶即可完成检测。在哑铃型DNA探针中,回文序列由两部分构成:一部分被设计为5'端悬垂瓣,可在FEN1存在时触发信号放大,并在FEN1缺失时阻止信号输出;另一部分作为5'悬垂瓣的互补序列,可在回文发夹辅助下,通过聚合酶和内切酶驱动启动四重等温扩增循环。这种“单瓣双功能”与“双酶四循环”的耦合集成,成功实现了荧光铜纳米粒的指数级信号放大,使FEN1检测的检出限低至3.5×10-6 U/mL。得益于其高选择性和抗干扰能力,该方法能根据细胞FEN1的检测结果明确区分癌细胞与正常细胞。该研究有望为分子诊断中的新型癌症标志物检测提供新思路。
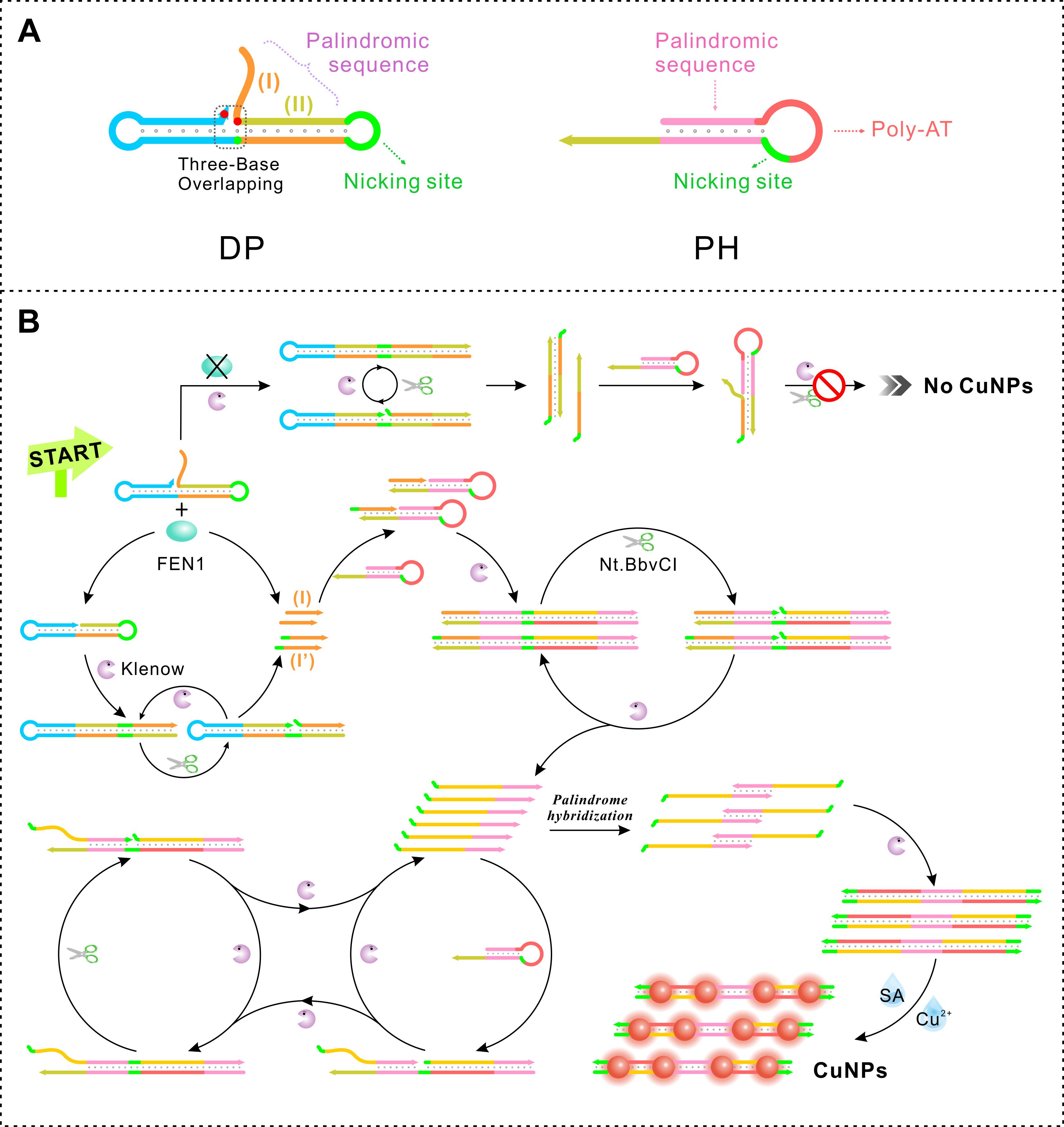
哑铃型探针和回文发夹序列设计及FEN1传感原理示意图
9月,Analytical Chemistry(《分析化学》)在线发表该团队研究成果,论文题为“Palindrome-Mediated Isothermal Cascade DNA Amplification and Effortless Nano-Signal Transduction for One-Pot and Ultrasensitive miRNA Sensing”(《回文介导等温级联DNA扩增与便捷纳米信号转导的miRNA超灵敏一锅法检测》)。我院2022级硕士研究生陈金涛为论文第一作者,陈金阳副教授为论文唯一通讯作者,湖北师范大学为论文唯一通讯单位。Analytical Chemistry是American Chemical Society(美国化学会)出版社旗下分析化学领域顶级期刊,中科院SCI化学大类一区TOP期刊、自然指数期刊,最新影响因子为6.7。

基于简单高效DNA等温扩增的超灵敏miRNA检测新方法研究对于推动精准分子诊断技术发展具有重要意义。该工作中,研究团队基于回文序列介导DNA恒温切刻/聚合级联扩增和荧光铜纳米粒(CuNPs)原位纳米信号转导,建立了一种超灵敏miRNA一锅检测新方法。得益于合理的回文序列设计,该检测方法具有较强的操作简便性,仅需两种DNA发夹探针和一对工具酶就能完成miRNA检测。高效的等温扩增和便捷的信号转导共同实现了对miRNA的超灵敏检测,方法检出限低,操作简单。得益于其高选择性和抗干扰能力,该方法能够根据细胞miRNA的检测结果明确区分癌细胞和正常细胞。此外,该方法仅需修改探针序列即可实现不同miRNA的检测,在新型分子诊断领域展现出优异的传感普适性与应用潜力。
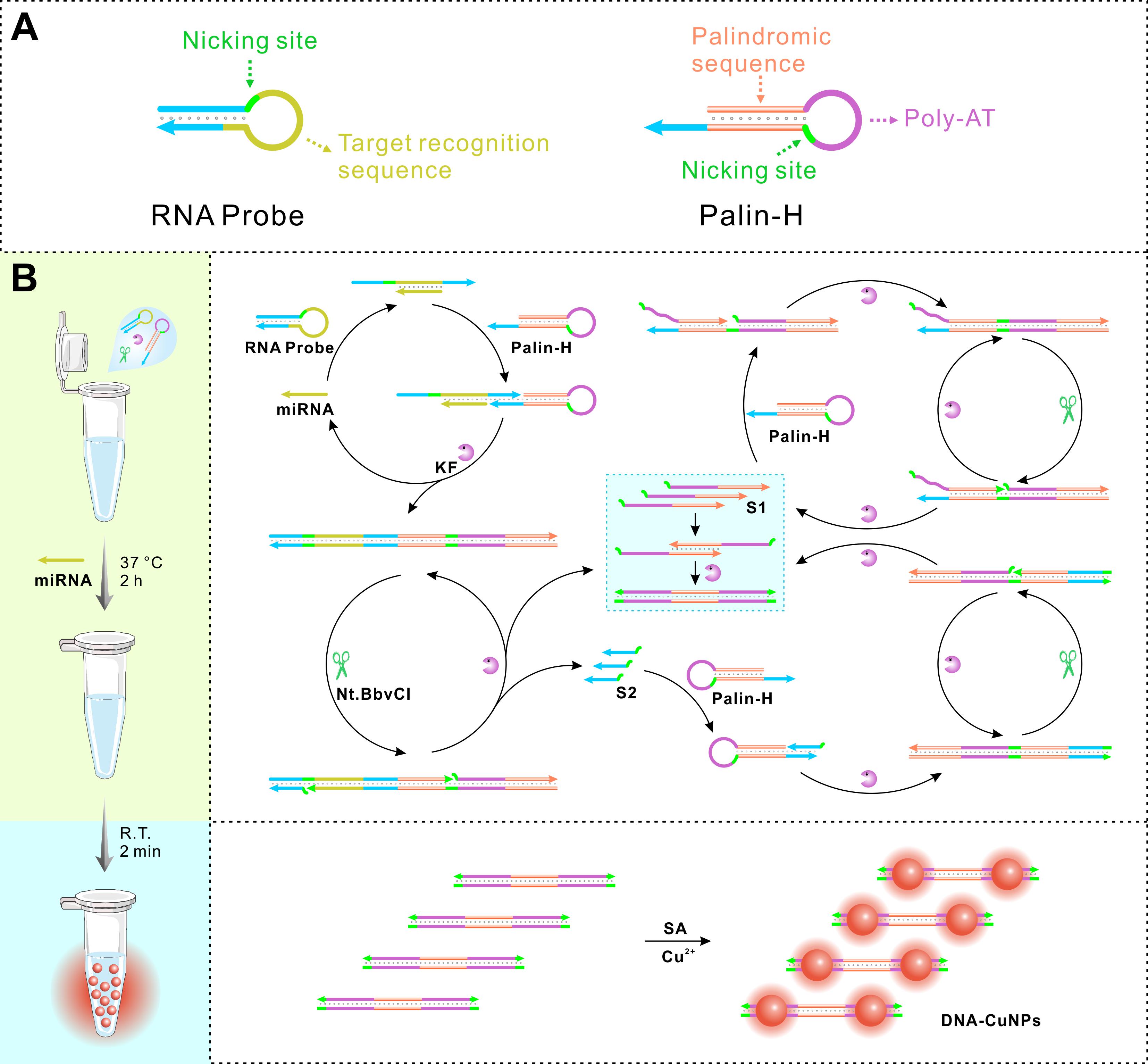
RNA探针和回文发夹结构设计及miRNA检测原理示意图
近日,Analytica Chimica Acta(《分析化学学报》)在线发表该团队研究成果,论文题为“All-in-one prepared highly stable fluorescent copper nanocluster composite for point-of-care sensing of tetracycline”(《一体化制备高稳荧光铜纳米簇复合材料用于四环素即时检测》)。我院2021级硕士研究生朱婷和2023级硕士研究生杨雨为论文共同第一作者,陈金阳副教授为论文唯一通讯作者,湖北师范大学为论文唯一通讯单位。

该工作中,研究团队通过一体化合成策略,制备了一种由二价锌聚集和纳米凝胶保护的半胱氨酸铜纳米簇复合材料(Zn-CuNCs@GC)。与铜纳米簇(CuNCs)相比,Zn-CuNCs@GC的荧光发射和荧光稳定性均有显著提高。此外,发现四环素能够与二价锌特异性结合形成TC-Zn(II)复合物,该复合物发出强烈的绿色荧光,并且同时解除了二价锌引起的CuNCs聚集效应,从而减弱了CuNCs的橙色荧光。基于这一发现,利用Zn-CuNCs@GC作为靶标识别和信号转导双功能元件,构建了一种用于四环素即时检测的荧光传感器。该传感器对四环素检测的灵敏度高,检出限为7.2 nM,且具有高选择性和抗干扰能力。基于智能手机比色分析,利用该传感策略还实现了高通量和可视化四环素检测,进一步展示了该传感器的便捷性和实用性。
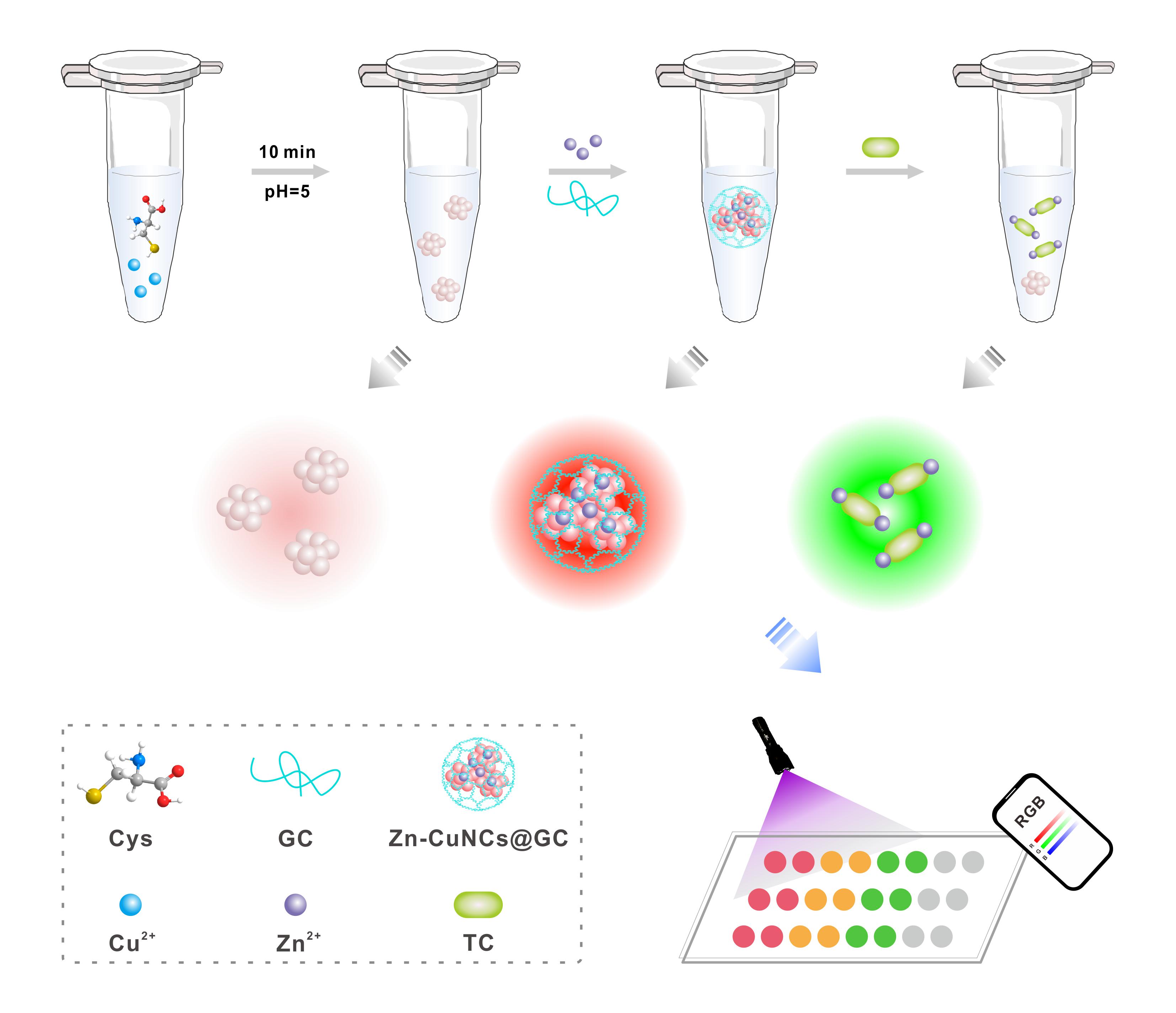
Zn-CuNCs@GC一体化合成及四环素传感原理示意图
以上工作得到国家自然科学基金青年项目(22004031)和湖北省自然科学基金面上项目(2023AFB996)等项目的资助。
论文信息:
1. Self-priming isothermal polymerization engineered in-situ copper nanoparticles generation for one-tube biomarkers sensing
Shasha Zeng1, Jintao Chen1, Chunjiao Qi, Guobin Mao, Yuhui Shang, Yu Yang, Jinyang Chen*
Analytica Chimica Acta, 2025, 1351, 343903
论文链接:https://doi.org/10.1016/j.aca.2025.343903
2. Palindrome design-guided “single-flap-double-duties” and “dual-enzymes-quadruple-cycles” enabled nano-signal amplification for customized FEN1 sensing
Jintao Chen1, Yuhui Shang1, Yu Yang, Yali Liu, Jinyang Chen*
Talanta, 2026, 297, 128642
论文链接:https://doi.org/10.1016/j.talanta.2025.128642
3. Palindrome-Mediated Isothermal Cascade DNA Amplification and Effortless Nano-Signal Transduction for One-Pot and Ultrasensitive miRNA Sensing
Jintao Chen, Yuhui Shang, Yu Yang, Yali Liu, Jinyang Chen*
Analytical Chemistry, 2025, DOI: 10.1021/acs.analchem.5c03949
论文链接:https://doi.org/10.1021/acs.analchem.5c03949
4. All-in-one prepared highly stable fluorescent copper nanocluster composite for point-of-care sensing of tetracycline
Ting Zhu1, Yu Yang1, Yuhui Shang, Yali Liu, Jinyang Chen*
Analytica Chimica Acta, 2025, 1377, 344688
论文链接:https://doi.org/10.1016/j.aca.2025.344688


